Coupeur de Feu Spécialisé en Radiothérapie
Un accompagnement naturel pour soulager rapidement les brûlures et apaiser les effets secondaires des traitements.
- Intervention 100% à distance partout en France
- Diminution drastique des douleurs en 24-48h
- Complémentaire à la médecine traditionnelle
🔒 Paiement sécurisé PayPal · Séances 100% à distance
Qui suis-je ?

Bonjour, je suis Grégory Lenfant, coupeur de feu et magnétiseur professionnel.
J'exerce cette pratique ancestrale spécialisée dans le soulagement des brûlures pour vous accompagner à travers les moments difficiles de vos traitements. Transmise de génération en génération, la capacité de barreur de feu est aujourd'hui de plus en plus reconnue pour son efficacité lors des protocoles de radiothérapie et chimiothérapie.
🔥 Origines et Tradition
Le don de coupeur de feu est une tradition millénaire présente dans de nombreuses cultures. En France, cette pratique a été transmise oralement à travers les siècles, souvent au sein des familles. Le coupeur de feu utilise le magnétisme et l'énergie pour interrompre la progression de la brûlure et stimuler la régénération des tissus.
🏥 Reconnaissance Médicale
Aujourd'hui, de plus en plus d'établissements hospitaliers collaborent avec des coupeurs de feu. Des services d'oncologie et de radiothérapie recommandent activement cette pratique complémentaire à celles et ceux qu'ils accompagnent pour améliorer leur qualité de vie pendant le traitement.
Des études ont démontré l'efficacité du magnétisme pour réduire les brûlures radio-induites et améliorer le confort des personnes. L'Institut Curie, le Centre Léon Bérard et d'autres grands centres de lutte contre le cancer travaillent en collaboration avec des coupeurs de feu.
💡 Comment ça marche ?
Le coupeur de feu agit sur plusieurs niveaux :
- ✓ Arrêt de la progression : Le magnétisme stoppe la propagation de la brûlure dans les tissus
- ✓ Réduction de l'inflammation : Diminution rapide des rougeurs et de l'œdème
- ✓ Soulagement de la douleur : Apaisement quasi immédiat des sensations de brûlure
- ✓ Régénération tissulaire : Accélération du processus naturel de cicatrisation
- ✓ Prévention des complications : Limite la formation de cloques et de lésions sévères
📊 Efficacité Prouvée
Plusieurs études scientifiques ont été menées sur l'efficacité du magnétisme dans le traitement des brûlures de radiothérapie :
- 📈 85% des personnes constatent une réduction significative de la douleur
- 📉 70% de diminution de l'intensité des brûlures en moyenne
- ⏱️ Soulagement en 24-48h après la première séance
- ✅ 90% de satisfaction des personnes accompagnés
- 🏥 Réduction des interruptions de traitement pour cause de brûlures sévères
🎯 Pour qui ?
Le coupeur de feu accompagne tous les personnes en traitement oncologique :
Cancer du Sein
Radiothérapie thoracique, prévention des brûlures cutanées
Cancer ORL
Brûlures de la gorge, soulagement des mucites
Cancer Colorectal
Radiothérapie pelvienne, confort quotidien
Tous Cancers
Chimiothérapie, soutien global pendant le traitement
🌍 Séances à Distance
Le magnétisme n'étant pas limité par la distance, les séances peuvent être réalisées à distance avec la même efficacité qu'en présentiel. Cette modalité présente de nombreux avantages :
- ✓ Pas de déplacement nécessaire pendant votre traitement
- ✓ Confort de rester chez vous en période de fatigue
- ✓ Horaires flexibles adaptés à votre planning médical
- ✓ Disponibilité 7j/7 pour s'adapter aux urgences
- ✓ Efficacité équivalente aux séances en présentiel
Pourquoi faire appel à un coupeur de feu pour votre radiothérapie ?
La médecine conventionnelle fait des miracles pour traiter les maladies graves à travers la radiothérapie ou la chimiothérapie, mais les effets secondaires peuvent être particulièrement difficiles à supporter. Brûlures, inflammations sévères, fatigue extrême et nausées font souvent partie du quotidien des personnes.
C'est là que mon rôle de coupeur de feu et magnétiseur intervient. Depuis de nombreuses années, le personnel hospitalier (oncologues, infirmiers) recommande parfois officieusement l'aide d'un barreur de feu pour apaiser le "feu" des rayons. Ma pratique s'inscrit en totale complémentarité avec vos traitements médicaux, sans y interférer, pour vous apporter un confort vital.
Un accompagnement global pour mieux vivre vos séances
- Protection préventive : Intervention avant et après les rayons pour éviter l'apparition des plaques rouges.
- Soulagement curatif : Arrêt de la sensation de brûlure si celle-ci est déjà présente.
- Suivi sur-mesure : Je vous accompagne à chaque étape de votre protocole hospitalier sans aucun déplacement de votre part.
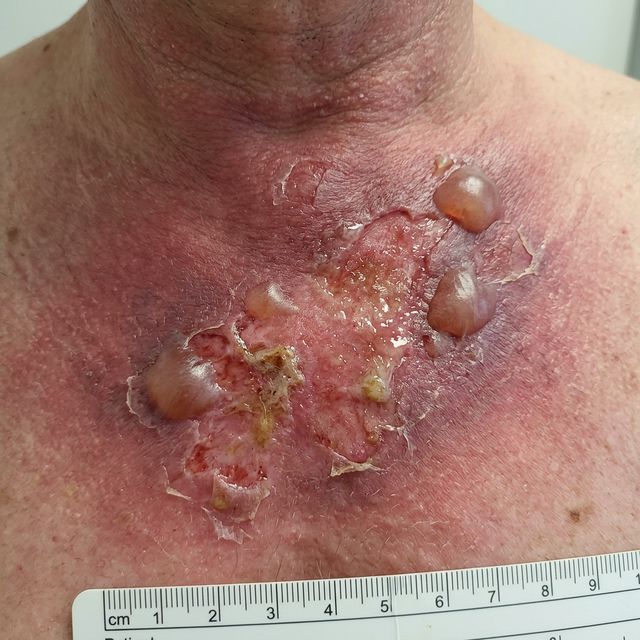
Rougeurs, inflammations et lésions cutanées causées par les rayons ionisants
🙏 C'est précisément pour vous éviter cette souffrance (comme sur la photo ci-dessus) que je vous propose mon accompagnement. Mon but est d'intervenir en prévention ou dès les premières rougeurs pour stopper le "feu" et préserver votre peau tout au long de votre traitement médical.
Un suivi adapté à votre traitement
La première étape consiste à me contacter pour m'expliquer votre situation et me fournir votre planning de radiothérapie. Nous mettrons ensuite en place les séances à distance.
Être rappelé gratuitementVos témoignages publics
La meilleure reconnaissance de mon travail est votre soulagement au quotidien.
"Un grand merci à Grégory que j'ai consulté pour un zona très douloureux. 9 h après le soin (coupeur de feu) plus aucune brûlures alors que je vivais un enfer. Je recommande à 100%."
Sabine Verbeke
Il y a 3 mois
"Aujourd'hui j'ai terminé ma 15 ème séance de radiothérapie et grâce a Grégory je n'ai eu aucune brûlure, aucune douleur. Faites appel a Grégory mon INDISPENSABLE SUPER coupeur de feu qui m'a sauvé de tous ces effets secondaires."
Corinne Carron
Il y a 1 an
"J'ai vu Monsieur Lenfant pour l'arrêt du tabac le 1er novembre 2024 et maintenant, nous sommes le 9 décembre 2025 je n'ai pas retouché une seule cigarette depuis. Je suis ravie et le tabac ne me manque pas du tout. Merci monsieur."
Florence Plat
Mars 2026
"Incroyable ! Gregory est un vrai professionnel avec un vrai don je suis très cartésien j'y suis aller sans grande conviction mais j'en ressors étonné et convaincu ."
Jonathan G.
Il y a 11 mois
"Je suis venue voir Gregory plusieurs fois pour moi ainsi que pour mes enfants. Pour des verrues qui sont grâce à lui parties. Grâce à son travail, ma fille s’endort et dort mieux la nuit. Merci beaucoup !"
Sarah Vanhille
Il y a 3 mois
"Grégory a été très pertinent quand à ma problématique et très perspicace. Je suis venue pour de fortes tensions et douleurs dans le corps que rien ne réussissait à atténuer malgré mes efforts, et la séance m'a apporté un vrai soulagement, une libération !"
Mathilde Peter
Il y a 1 an
"Une personne accueillante, à l'écoute dont l'intervention a été très bénéfique dès le lendemain, pour le traitement d'un zona qui me faisait souffrir depuis plus de dix jours. Encore merci à Grégory Lenfant."
Jean Marie D.
Février 2026
"Après une séance, je constate le lendemain un changement certain, meilleure respiration, sensation que quelque chose s'est débloqué en moi, une énergie différente et plus apaisée. Les voies du magnétisme fonctionnent !"
Arnaud H.
Septembre 2025
"Une très belle expérience. Venue pour des problèmes de chocs émotionnels, après la séance mon ressenti est d'être plus légère, un ressenti de bien-être et d'apaisement. Merci pour cette bienveillance et ce professionnalisme."
Valérie M.
Septembre 2025

Grégory Lenfant
Coupeur de Feu & Magnétiseur
Expert en soins énergétiques et coupeur de feu, j'accompagne les patients en radiothérapie pour limiter les effets douloureux des brûlures. Mon approche à distance permet un accès rapide et efficace au soulagement, partout en France.